13/11/2009
Diversidade do Influenza e o rearranjo
Uma das características mais importantes do Influenza a ser considerada no preparo para pandemias é o rearranjo. Uma mistura de genes de dois ou mais vírus diferentes capaz de gerar uma variedade nova. Como o novo Influenza A (H1N1).
![]() Embora as mutações tenham um papel importante na diversidade do Influenza, e contribuam bastante para que tenhamos de desenvolver novas vacinas anualmente, o rearranjo causa uma variação antigênica brusca (antigenic shift) que pode gerar um vírus completamente novo para nosso sistema imune.
Embora as mutações tenham um papel importante na diversidade do Influenza, e contribuam bastante para que tenhamos de desenvolver novas vacinas anualmente, o rearranjo causa uma variação antigênica brusca (antigenic shift) que pode gerar um vírus completamente novo para nosso sistema imune.
O rearranjo é uma decorrência do ciclo do Influenza e de seus 8 genes. Quando o vírus entra na célula, seus genes se replicam no núcleo e saem dele para o citoplasma para poderem ser empacotados. Todos os 8 genes precisam entrar na nova partícula viral formada para que ela seja infectiva. Para isso, cada gene possui uma sequência sinal que interage com a proteína M1, que dá a estrutura da partícula viral. Mas este sinal é parecido mesmo em vírus distintos, e os genes de um podem ser empacotados junto de genes de outro.
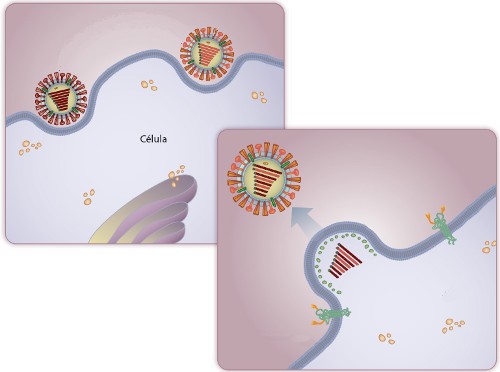
Quando dois Influenzas diferentes entram em uma mesma célula, seus genes podem se rearranjar na formação de novas partículas virais.
Com isso, nos raros eventos – raros em relação à infecções por um só vírus – em que dois Influenza diferentes entram na mesma célula, diferentes mosaicos de genes podem ser formados nas partículas que sairão. A maioria destas combinações não será viável, mas algumas entre as milhares podem ser infecciosas, e uma porcentagem menor ainda pode ser mais infecciosa do que os vírus originais. Este é o rearranjo.
A loteria do rearranjo, onde os genes são embaralhados e sorteados, pode originar linhagens de Influenza muito perigosas. Basta pensar na possibilidade do H5N1 altamente patogênico adquirir genes que o ajudem a se espalhar com mais eficiência, ou no caso do Influenza A (H1N1) adquirir genes que aumentem a gravidade da gripe que ele causa.
É desta forma que o Influenza tem se rearranjado e misturado genes em aves, porcos e humanos. E dado o estrago causado por estas variantes híbridas, este é um evento fundamental no surgimento de linhagens pandêmicas. O rearranjo tem a vantagem de trazer para seu genoma componentes inéditos.
Genes de vírus de mamíferos que já estão otimizados para crescer em uma temperatura corpórea do hospedeiro de cerca de 37°C, contra cerca de 40°C em aves, se misturam com novos HA e NA aviários que não serão nem um pouco reconhecidos pelo anticorpos. Uma mudança muito maior do que as mutações. Os porcos possuem um papel importante aqui. Eles não só convivem entre humanos e aves de criação como possuem ambos os tipos de receptor de membrana. Assim, podem ser infectados com vírus aviários e humanos e fornecer um ambiente com condições para que o híbrido se adapte ao nosso metabolismo.
São eventos como estes que deram origem aos vírus que causaram a maioria das pandemias de gripe. Embora o H1N1 de 1918 pareça ser um vírus que veio diretamente de aves para humanos – independente de ter passado por porcos antes ou não, provavelmente foi transmitido como um vírus inteiro – em 1957, um evento de rearranjo com um vírus aviário forneceu novas HA e NA que permitiram que o vírus causasse muito mais estrago, na chamada Gripe Asiática. Em 1968, novamente em um rearranjo, o vírus adquiriu uma nova Hemaglutinina aviária e causou a Gripe de Hong Kong.
Mesmo eventos de rearranjo dentro de uma mesma linhagem são capazes de causar doenças mais severas e falha na cobertura da vacina, como os surtos de gripe de 1947, 1851, 1997 e 2003. Os dois primeiros foram eventos decorrentes de rearranjos do H1N1 e os dois últimos do H3N2 humanos.
Agora em 2009 vivemos outro reflexo do rearranjo, desta vez em vírus suínos. Em 1918 o H1N1 aviário passou a circular tanto em humanos quanto em porcos, gerando linhagens distintas e presentes até hoje. Em 1997, um novo vírus suíno surgiu na América do Norte, de um triplo rearranjo, com uma combinação de genes de Influenza humanos (nosso H3N2 gerado em 1968), suínos e aviários. Trata-se do H1N2 suíno. – Os porcos da Europa estavam virtualmente livres de gripe até 1976, quando o H1N1 suíno foi trazido em um carregamento de porcos da América do Norte. Este foi rapidamente substituído por um H1N1 aviário em 1979.
Por fim, em 2008, o triplo rearranjado circulante em porcos na América do Norte se rearranjou novamente, com o vírus suíno H1N1 da Eurásia. Ainda não se sabe se este evento ocorreu em porcos ou em humanos. O mais provável é que tenha ocorrido em humanos, uma vez que ainda não encontramos porcos contaminados. Este novo Influenza A (H1N1) contaminou humanos e está causando a atual pandemia.
Fontes:
Palese, P. (2004). Influenza: old and new threats Nature Medicine, 10 (12s) DOI: 10.1038/nm1141
10.1056/NEJMp0904819
Morens, D., Taubenberger, J., & Fauci, A. (2009). The Persistent Legacy of the 1918 Influenza Virus New England Journal of Medicine, 361 (3), 225-229 DOI: 10.1056/NEJMp0904819
4 Comentários » Postado em: Pandemia, evolução, origem


Recebi isso no SEMCIÊNCIA:
cláudio deixou um novo comentário sobre a sua postagem “Gripe Suà na: a segunda onda “:
Algum colega pode explicar o sentido deste parágrafo?
“The concept of acquisition via recombination has serious implications for the current pandemic. It was used to predict the D225G change, in part because the change was “in play” and appearing in July/August sequences at increasing frequency, even though the H1N1 sequences represented different genetic backgrounds. Similarly the clusters of Tamiflu resistance in Wales and North Carolina are also driven by recombination, as happened when the identical change was acquired in H1N1 seasonal flu in patients who were not taking Tamiflu (oseltamivir).
Thus, the concept of recombination predicts that the D225G receptor binding domain change, and the H274Y Tamiflu resistance change, which continue to spread via recombination”.
Cláudio
Osame,
Ele fala sobre a mutação que muda o tropismo do vírus, dirigindo ele mais fundo no pulmão e causando sintomas mais severos. E sugere que isso pode ser espalhado por recombinação. Ainda confio na seleção natural, a não ser que esta mutação favoreça o vírus portador de alguma forma, ele não será transmitido facilmente. E não sei de nada que suporte ou refute a idéia de que ela favorece.
Quanto à resistência ao Oseltamivir, essa eu acho mais perigosa, dado que ela realmente favorece o vírus portador em um ambiente saturado de antiviral, mas ela ainda depende de uma outra mutação para restaurar a atividade, e o vírus ainda continua suscetível ao zanamivir. O que alivia mas não acaba com a preocupação.
[...] Por mais que pareça estranho anticorpos contra linhagens humanas serem eficazes contra vírus suínos, uma recapitulada na história de nossas gripes mostra que isso não é nada absurdo. Tanto humanos quanto porcos foram infectados por uma linhagem aviária pouco antes de 1918, que desde então tem evoluído em paralelo, com alguns encontros ocasionais. [...]
[...] está presente nesta célula, os vírus formados são mosaicos de genes de origem diferentes. Este processo foi explicado em mais detalhes aqui. O rearranjo é preocupante pois o vírus que ele origina possui mudanças muito mais abruptas do [...]